Regulation und Funktion von TGF-ß-Signalen in der frühen Embryonalentwicklung
Forschungsbericht (importiert) 2007 - Max-Planck-Institut für Immunbiologie und Epigenetik
Einleitung
In der Embryonalentwicklung wird eine Vielzahl an Zellarten zeitlich und räumlich koordiniert gebildet. Dabei spielen Wachstumsfaktoren eine zentrale Rolle. Sie werden in den extrazellulären Raum abgegeben und stimulieren durch die Bindung an membranständige Rezeptoren intrazelluläre Signalkaskaden, die Genexpression steuern. Diese signalabhängige Regulation der Genexpression erlaubt die Koordinierung von Zellproliferation, Zellwanderung und Zelldifferenzierung in komplexen Geweben, insbesondere da Zellen unterschiedlich auf das Signal reagieren, je nachdem welche Kombinationen an Rezeptoren und intrazellulären Mediatoren in der Zelle vorliegen. Der TGF-ß-Signalübertragungsweg ist von zentraler Bedeutung für die Determinierung verschiedener Zelltypen in der Embryonalentwicklung von Wirbeltieren. Aber auch im erwachsenen Organismus ist eine präzise Steuerung von TGF-ß-Signalen notwendig, besonders weil Mutationen in Komponenten der TGF-ß-Signalkaskade zur Bildung von malignen Tumoren führen [1].
Der TGF-ß-Signalübertragungsweg
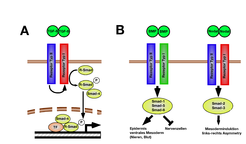
Proteine der TGF-ß-Familie binden an Proteinkomplexe in der Zellmembran, die aus den so genannten Typ II- und Typ I-Rezeptoren bestehen. Die Bindung des TGF-ß-Liganden stimuliert die Aktivierung des Typ I-Rezeptors durch den Typ II-Rezeptor. Der aktivierte Typ I-Rezeptor phosphoryliert und aktiviert intrazelluläre Proteine der SMAD-Familie, die Rezeptor assoziierten Smads (R-Smads). Diese binden nun an Smad-4 und steuern im Zellkern zusammen mit einer Reihe zusätzlicher Transkriptionsfaktoren (TF) spezifische Gentranskription (Abb. 1A).
Die TGF-ß-Familie kann dabei in zwei Gruppen eingeteilt werden, die Bone morphogenetic protein-Gruppe (BMP) und die Nodal-Gruppe. Die BMP-Gruppe aktiviert mithilfe spezifischer Typ I-Rezeptoren die R-Smads Smad-1, Smad-5 und Smad-8, während die Nodal-Gruppe Smad-2 und Smad-3 aktiviert [2]. Durch die Aktivierung spezifischer Smad-Proteine stimulieren die beiden TGF-ß-Gruppen sehr unterschiedliche Prozesse. In der frühen Embryonalentwicklung sind Nodal-Proteine vor allem für die Bildung des Mesoderms notwendig, aus dem ein Großteil der inneren Organe entsteht. BMP-Signale hemmen die Bildung von Nervengewebe und stimulieren die Bildung von Epidermis (Haut) und ventralem Mesoderm, aus dem z.B. Nieren und Blut hervorgehen (Abb. 1B)
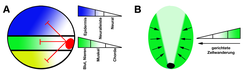
Die Regulation der Genexpression durch TGF-ß-Signale ist sehr Dosis-abhängig. Bereits kleine Variationen in der BMP- oder Nodal-Konzentration stimulieren die Bildung verschiedener embryonaler Gewebe. Daher gibt es eine Vielzahl an Mechanismen, durch die TGF-ß-Signale innerhalb und außerhalb der Zelle reguliert werden. Von besonderem Interesse ist die Regulation von BMP-Signalen im extrazellulären Raum. Genetische Studien im Fischembryo und funktionelle wie auch biochemische Analysen im Froschembryo haben ein sehr komplexes Netzwerk aus Protein-Protein-Wechselwirkungen identifiziert, durch die die Bindung von BMPs an BMP-Rezeptorkomplexe reguliert wird, einschließlich des BMP-Antagonisten Chordin, Metalloproteinasen der Tolloid-Familie, sowie Twisted Gastrulation und Sizzled [2, 3]. Der BMP-Antagonist Chordin bindet BMPs und hemmt dadurch die Interaktion von BMPs mit Rezeptorkomplexen. Diese Hemmung ist reversibel, da Tolloid Chordin spalten und BMP wieder freisetzen kann. Twisted gastrulation stimuliert die Bindung von Chordin an BMP wie auch die Spaltung von Chordin durch Tolloid, während Sizzled die proteolytische Spaltung von Chordin durch Tolloid hemmt. Verschiedene Komponenten dieses Netzwerks wurden in Mensch, Maus und Frosch, aber auch in Fliege und Seeanemone gefunden. Dabei stellte man fest, dass – trotz der Unterschiede in den sich bildenden Strukturen – zumindest einige Proteine dieses regulatorischen Netzwerkes vergleichbare Funktionen ausüben [4, 5, 6]. Während der frühen Embryogenese wird Chordin im Frosch, wie auch im Fisch oder der Maus, lokal sezerniert und generiert dadurch einen BMP-Signalgradienten. Dieser Gradient wird im Embryo auf verschiedene Weise interpretiert. Zum einen werden Zelltypen konzentrationsabhängig determiniert. Zum anderen steuert der Gradient gerichtete Zellbewegungen [7], durch die aus dem kugelförmigen Ei ein länglicher Embryo geformt wird (Abb. 2).
Identifizierung von BMP-Zielgenen
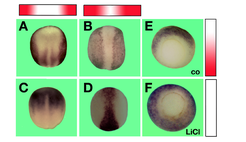
Der südafrikanische Krallenfrosch Xenopus laevis wird häufig für die Analyse von Signalkaskaden und deren Wechselwirkung mit bekannten oder neuen Proteinen eingesetzt. Die Froscheier sind sehr groß (1.5 mm im Durchmesser) und ermöglichen eine Vielzahl embryologischer Manipulationen. Zusätzlich legt ein Weibchen über 2000 Eier am Tag, die eine fast unerschöpfliche Quelle für die Isolation von DNA, RNA oder Proteinen darstellen. Durch Mikroinjektion von frühen Froschembryonen mit synthetischer mRNA oder chemischer Behandlung, z.B. mit Lithiumchlorid, können Signale stimuliert oder gehemmt werden und ausreichende Mengen an RNA aus verschiedenen embryonalen Stadien isoliert werden, die eine vergleichende Analyse mithilfe von Mikroarray-Chips erlauben. Die Arbeitsgruppe um Michael Oelgeschläger hat eine Reihe von neuen Genen identifiziert, die durch BMP-Signale transkriptional reguliert werden und verschiedene BMP-Aktivitäten im frühen Froschembryo vermitteln. Dafür wurde RNA aus frühen Froschembryonen isoliert, in denen BMP-Aktivität durch Mikroinjektion synthetischer mRNA oder chemischer Behandlung entweder stimuliert oder gehemmt worden war und mithilfe von Mikroarray-Analysen verglichen. Die Expression der isolierten Gene korrelierte dabei sehr gut mit BMP-Aktivität. Vor allem in frühen Embryonalstadien wird der BMP-Signalgradient durch die Expression dieser Gene deutlich sichtbar. BMP-Signalgradienten determinieren während der Gastrulation, in der Mesoderm in den Embryo einwandert, die dorsal-ventrale (Rücken-Bauch) Körperachse. In der dorsalen oder Rückenseite des Embryos wird während der Neurulation die Neuralplatte gebildet, aus der das zentrale Nervensystem hervorgeht. Da in der Neuralplatte kaum BMP-Aktivität nachzuweisen ist, werden in diesem Bereich vor allem Gene transkribiert, deren Expression durch BMP- Signale gehemmt wird, während Transkripte BMP-aktivierter Gene von der Neuralplatte ausgeschlossen sind. (Abb. 3).
Eines der Gene, die durch BMP-Signale in ihrer Expression gehemmt werden, kodiert für ein Transmembranprotein, xTspan-1. Durch Mikroinjektion synthetischer mRNA konnte gezeigt werden, dass xTspan-1 Zelladhäsion und Zellmigration reguliert [8]. Dies wurde unter anderem durch sogenannte Reaggrations-Assays nachgewiesen. Dafür wurde ein Aggregat aus unbehandelten embryonalen Zellen und xTspan-1 injizierten Zellen, die zusätzlich einen fluoreszierenden Marker exprimierten, hergestellt. Die xTspan-1-positiven Zellen mischten sich nicht mit den unbehandelten Zellen, sondern sammelten sich an der Oberfläche des Aggregats an. Dieser Effekt konnte durch Ko-Injektion von mRNAs, die für Zelladhäsionsproteine der Cadherin-Familie kodierten, aufgehoben werden. Diese Ergebnisse weisen auf eine Hemmung der Zelladhäsion durch xTspan-1 hin, die unter anderem durch reduzierte Cadherin-Aktivität in den xTspan-1 exprimierenden Zellen erklärt werden kann. Zusätzlich wurde mithilfe von Morpholino-Oligomeren, die spezifisch die Proteinsynthese von endogenem xTspan-1 hemmen, nachgewiesen, dass xTspan-1 für die Differenzierung von neuronalen Vorläuferzellen notwendig ist (Abb. 4).

Dieses Protein ist also an den oben beschriebenen BMP-abhängigen Prozessen beteiligt und stellt eines der ersten BMP-regulierten Gene dar, das sowohl Zellbewegungen als auch die Differenzierung von Nervenzellen regulieren kann.
Ausblick
Diese Arbeiten haben zur Identifizierung einer Vielzahl neuer BMP-regulierter Gene geführt, einschließlich Tspan-1, das an der Regulation von Zellbewegungen und der Differenzierung von Nervenzellen beteiligt ist. Die weitere Analyse dieser Gene wird unser Verständnis für die molekularen Mechanismen, durch die BMP-Signale eine Vielzahl an biologischen Aktivitäten in der Embryogenese wie auch im adulten Organismus steuern, weiter vertiefen. Die überraschend ausgeprägte Ähnlichkeit von BMP-Aktivitäten in verschiedenen Wirbeltierarten lässt erwarten, dass homologe Gene in Säugetieren, einschließlich des Menschen, vergleichbare Funktionen ausüben.



