Mechanismen alternativer RNA-Prozessierung in Neuronen
Labor Hilgers
Ein Ziel unseres Labors besteht darin, mechanistische Einblicke in die ko-transkriptionellen Prozesse zu erhalten, die die Neuronen-spezifischen RNA-Sequenzen im Nervensystem hervorrufen.
In Metazoen exprimieren die meisten Gene multiple Transkriptions-Isoformen durch die Verwendung alternativer Polyadenylierungsstellen (poly(A)), die das Ende der Transkription signalisieren. In Tieren von Fliegen bis Menschen erfahren Hunderte von Genen ausschließlich in Neuronen eine Verschiebung zur distalen Stelle poly(A), wodurch manchmal extrem lange 3’UTRs entstehen.
Wir fanden heraus, dass das hoch konservierte neuronale RNA-bindende Protein ELAV global alle Stellen der neuronalen 3’Ende-Prozessierung reguliert und in vivo direkt an die proximalen Polyadenylierungsstellen der Ziel-mRNAs bindet. ELAV reguliert auch das Neuronen-spezifische alternative Splicing und stellt tatsächlich den zentralen Effektor Neuronen-spezifischer Transkriptom-Signaturen dar.
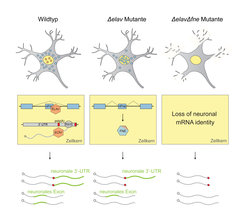
Diese Monopolfunktion von ELAV kann bei Beeinträchtigung von ELAV durch sein Paralog FNE übernommen werden: in elav-Mutanten dringt das normalerweise cytoplasmische Protein FNE in den Nukleus ein und übernimmt die Funktion von ELAV in einem neuen, „Exon-Activated functional Rescue“ (EXAR) genannten, Prozess. Neuronen, denen beide Proteine ELAV und FNE fehlen, verlieren ihre neuronalen RNA-Signaturen vollständig.
Wir konzentrieren uns jetzt auf genregulierende Mechanismen, die zur Entstehung diverser Neuronen-spezifischer RNA-Sequenzen einschließlich ultralanger 3’UTRs, Neuronen-spezifischer Exons, und zirkulärer RNAs, führen.
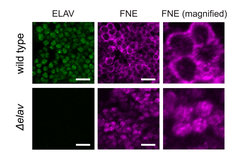
Aktiviertes FNE dringt nur bei Fehlen von ELAV in den Nukleus ein. Mikroskopische Aufnahme neuronaler Zellen in Drosophila-Embryonen. Die Proteine ELAV und FNE wurden durch Immunhistochemie sichtbar gemacht. Maßstab: 10µm.
Unsere vorangehende Arbeit deckte eine unerwartete Verbindung zwischen der Initiierung der Transkription und alternativer mRNA-Prozessierung auf: ELAV bindet an Promotorregionen seiner Zielgene und diese Bindung wird durch das promotor-proximale Pausieren der RNA Polymerase II (Pol II) unterstützt. Wie ELAV beim Initiieren der Transkription die RNA-Prozessierung, viele Kilobasenpaare weiter, beeinflusst, bleibt ein Rätsel.
Wir vermuten, dass epigenetische Marker, Promotorsequenz und das Pausieren von Pol II mit der ELAV-Aktivität zusammenwirken, um die Expression Neuronen-spezifischer RNAs zu begünstigen. Um die regulatorischen Verbindungen zwischen transkriptionellen, ko- und post-transkriptionellen Prozessen zu untersuchen, setzen wir sowohl funktionale Genetik, RNA-Biochemie und Proteomik, als auch die whole-genome-Transkriptomik einschließlich ChIP, CLIP und Ultra-long-read-Sequenzierung ein.

