Drosophila
Forschungshighlights mit einem unerwarteten Modellorganismus
Warum Drosophila? | Interaktiver Besuch im Fliegenlabor | Fliegenforschung am Institut
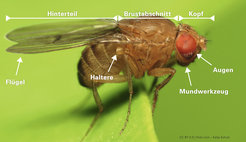
Drosophila melanogaster besitzt am Brustabschnitt 3 Beinpaare und gehört zu den Zweiflüglern, da sie eigentlich 2 Flügelpaare besitzen. Aber davon ist nur eines tatsächlich ein Flügelpaar. Die Hinterflügel sind zu Schwingkölbchen, den sogenannten Halteren umgebildet.
Fruchtfliegen, auch bekannt als Tau- oder Essigfliegen, sind für die meisten von uns nichts anderes als kleine Störenfriede, die sich im Sommer in unseren Küchen vermehren. Viele Wissenschaftler:innen, auch am MPI für Immunbiologie und Epigenetik, sehen das jedoch ganz anders.
Drosophila melanogaster, wie die gemeine Fruchtfliege in Laboren weltweit genannt wird, gehört nämlich zu den am besten erforschten Organismen in der Biologie und war maßgeblich für viele bahnbrechende Entdeckungen auf dem Gebiet der Genetik, Entwicklungsbiologie. Auch viele Erkenntnisse der modernen Medizin basieren auf Grundlagen, die durch die Fliegenforschung gelegt wurden. Mithilfe von Studien in Drosophila melanogaster wurde bisher nicht nur die Chromosomentheorie der Vererbung entwickelt (Nobelpreis an Thomas H. Morgan 1933), sondern fünf weitere Nobelpreise gingen an Forscher:innen, die ihre bahnbrechenden Entdeckungen in Drosophila gemacht haben.
Warum ist Drosophila als Modellorganismus so beliebt?
Fruchtfliegen bringt ideale Vorrausetzungen für die Haltung mit. Sie brauchen nicht viel Platz und haben keine hohen Ansprüche an ihre Umgebung: ein kleines Plastik- oder Glasgefäß und die passende Nahrung genügen. Passende Temperaturen und Luftfeuchtigkeit stellen sicher, dass die Tiere sich problemlos halten und vermehren. Stichwort: Vermehrung. Unter optimalen Bedingungen legt ein Drosophila-Weibchen bis zu 100 Eier pro Tag. Aufgrund der schnellen Entwicklung vom Ei zur ausgewachsenen Fliege binnen 10 Tagen sowie ihre hohe Nachkommenzahl stehen den Forscher:innen innerhalb kürzester Zeit eine große Zahl an Tieren zur Verfügung. Pro Jahr können so rund 25 (!) Fliegen-Generationen heranwachsen. Zum Vergleich: Labormäuse bringen pro Jahr lediglich vier bis sechs Generationen hervor.

Von Vorteil ist außerdem, dass die Tier trotz ihrer geringen Größe vergleichsweise leicht zu untersuchen sind. Da die Fliegen Eier legen, entwickelt sich der Nachwuchs außerhalb des Körpers der Mutter und so können die Forscher:innen den entwickelnden Embryo leichter beobachten und genetisch verändern. Das Erbmaterial besteht aus nur 8 Chromosomen (zum Vergleich: Maus 40 Chromosomen, Mensch 46 Chromosmen), die in den Speicheldrüsen der Insekten besonders groß als Riesenchromosomen ausgebildet sind. So erleichtert die Fruchtfliege trotz ihrer geringen Größe die genetische Forschung enorm.
Äußerlich haben Fruchtfliege und Mensch nicht viel gemeinsam. Umso erstaunlicher ist es, dass ungefähr 60 Prozent der Fliegen-Gene beim Menschen in ähnlicher Form vorkommen und von den 289 Genen, die Krankheiten beim Menschen verursachen können, existieren 177 entsprechende Varianten auch bei der Fliege. Dank dieser hohen genetischen Ähnlichkeit können Wissenschaftler an den Fliegen untersuchen, welche Funktion Gene besitzen, die beim Menschen Krankheiten hervorrufen können.
Lesen Sie mehr über die Fruchtfliege als Modellorganismus in biologischen Forschung auf den Themenseiten zum Modellorganismus Fliege der Max-Planck-Gesellschaft.
Besuchen Sie unser Fliegenlabor
In dieser interaktiven Dokumentation gibt Dr. Plamen Georgiev, Leiter unseres Fliegenlabors, exklusive Einblicke in seine Arbeit. Unter anderem erklärt er, wie Fliegen im Labor gefüttert werden und warum sie sich hervorragend für genetische Manipulationen eignen. Außerdem sprechen Nutzer:innen der Einrichtung über ihre Forschung mit der Fliege und teilen ihre besten „Fliegengeschichten“.
Dieses Projekt entstand in Zusammenarbeit mit Studierenden der Hochschule Offenburg: Artur Bauer, Sven Heper, Konradin Köchling und Maxim Maier. Die Erstellung einer interaktiven Dokumentation zum Thema Mensch-Tier-Interaktionen war eine Semesterarbeit in der Lehrveranstaltung „Medientexte“ (2015) von Prof. Daniel Fetzner.
Fliegenforschung an unserem Institut
Dosiskompensation (Labor Akhtar)
Frauen haben zwei Kopien des X-Chromosoms mit über 1.000 Genen. Männer besitzen hingegen nur eine Kopie und stattdessen ein genarmes Y-Chromosom. Dieses Chromosomen-Ungleichgewicht findet sich auch bei vielen weiteren Arten im Tierreich. Es ist jedoch überlebenswichtig, diese Unterschiede „auszugleichen“, um dieselbe „Gendosis“ zu erzielen. Beim Mensch und bei der Maus schalten die Weibchen eines ihrer X-Chromosomen einfach ab. Bei der Fruchtfliege Drosophila übernimmt das Männchen die Arbeit. Ein epigenetischer Faktor, der als MSL-Komplex bezeichnet wird, bindet an das einzelne männliche X-Chromosom und hyperaktiviert es.
Erkenntnisse zu diesen Prozessen und den beteiligten Molekülen helfen nicht nur die Mechanismen der Dosiskompensation in Fliege, Maus und Mensch zu verstehen, sondern tragen auch erheblich zum besseren Verständnis der Genregulation allgemein bei. Erkenntnisse aus der Grundlagenforschung des Instituts waren so zum Beispiel zentral für die Entschlüsselung der molekularbiologische Ursache für eine seltene Erkrankung, bei der betroffene Kinder unter starken Entwicklungsverzögerungen leiden. Lesen Sie dazu mehr in den Pressemitteilungen des Instituts.
Epigenetische Vererbung (Labor Iovino)
Wir sind mehr als die Summe unserer Gene. Epigenetische Mechanismen, die durch Umwelteinflüsse wie Ernährung, Krankheit oder unseren Lebensstil verändert werden, nehmen eine wichtige Rolle bei der Steuerung unseres Erbguts ein, indem sie Gene ein- oder ausschalten. Lange Zeit war fraglich, ob diese epigenetischen Informationen, die sich über das ganze Leben hinweg in unseren Zellen ansammeln, die Grenze der Generationen überschreiten und an Kinder oder sogar Enkel weitervererbt werden können. Forscherinnen des MPI konnten mithilfe von Drosophila zeigen, des Max-Planck-Instituts für Immunbiologie und Epigenetik in Freiburg konnten nun zeigen, dass nicht nur die vererbte DNA selbst, sondern auch vererbte epigenetische Instruktionen zur Regulierung der Genexpression der Nachkommen beitragen.
Eine epigenetische Modifikation namens H3K27me3 wird so nicht nur durch die mütterliche Keimbahn auf den Nachwuchs übertragen wird, sondern steuert auch einen fein abgestimmten Mechanismus, der für die Genomaktivierung während der frühen Embryogenese der Fliege erforderlich ist.
Dicke Fliegen (ehm. Labor Pospisilik)
Wissenschaftler:innen am MPI konnten zeigen, dass Fruchtfliegen Änderungen ihres Stoffwechsels vom Vater auf den Sohn vererben. Ein zuckerreiches Festmahl vor der Paarung kann so für eine Fruchtfliege und ihren Nachwuchs Folgen haben: Die Fliegenkinder werden dann nämlich anfälliger für Übergewicht. Die Ernährung der Väter aktiviert Gene, die das Erbgut epigenetisch verändern können. Diese Veränderungen werden vererbt und steuern in der nächsten Generation die Aktivität von Genen für den Fettstoffwechsel.
Die Forscher:innen haben darüber hinaus ein ähnliches Gen-Netzwerk auch bei Menschen und Mäusen gefunden, das die Anfälligkeit für Übergewicht erhöht. Dazu wurden Daten von Untersuchungen an Pima-Indianern – einem Stamm nordamerikanischer Ureinwohner, deren Angehörige häufig unter Übergewicht leiden – sowie eineiigen Zwillingen ausgewertet. Demnach besitzen übergewichtige Menschen dieselbe Gen-Signatur wie die Fruchtfliegen. Die Anfälligkeit für ein hohes Körpergewicht steigt also auch beim Menschen, wenn bestimmte Gene epigenetisch verändert werden.